
순수물질의 상변화는 뚜렷하고 일정하며 열역학에서는 비체적의 변화가 가장 큰 액체와 기체 사이에서의 상변화에 관점을 두고 있다.
순수 물질의 상변화 과정
상변화 관계
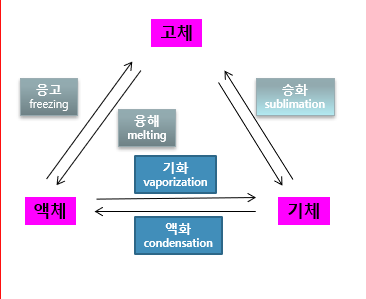
<그림 1> 상변화 관계
◇ 기화(Vaporization) 종류
▶ 증발(Evaporation) : 끓는점 아래에서 표면 기화(100℃ 미만에서 물의 증발)
▶ 비등(Boiling) : 끓는점 이상에서 액체 전체 기화(100℃ 이상에서 물의 비등)
▶ 승화(Sublimation) : 고체상태의 기화(상온 상압 드라이아이스 승화)
▶ 플래쉬(Flash) : 포화액체의 압력이 낮아져 순간적인 기화 (기화 후 포화상태의 온도 낮아짐)
순수물질의 상변화 과정(일정 압력)
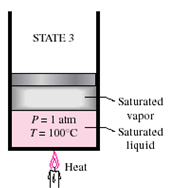
20℃, 1기압의 액체 물이 들어 있는 피스톤과 실린더 시스템의 가열에 따른 상태변화는 다음 그림 2와 같다.
 |
 |
 |
 |
 |
| 압축액 | 포화액 | 포화액-증기혼합물 | 포화증기 | 과열증기 |
<그림 2> 가열에 따른 상태변화(일정 압력)
1. 압축액 (Compressed liquid) :
20℃ 1기압의 물은 액상으로 존재하는데 이를 압축액(compressed liquid) 혹은 과냉액(subcooled liquid)라 함.
⇒ 열을 가해도 쉽게 기체 상태로 증발하지 않는 액체
1) 액체의 온도는 주어진 압력에서의 포화온도보다 낮다.
⇒ Tw < Tsat (Tw=20℃, Tsat =100℃@1 atm)
2) quality(건도, 건분, 질) : 의미가 없다.
2. 포화액 (Saturated liquid) :
포화온도와 압력하에 있는 액체
⇒ 열을 가하면 쉽게 기체 상태로 증발하는 액체 (liquid which is about to vaporize)
1) Tw = Tsat =100℃ @1atm
2) quality : x = 0 (건도 0%)
3) 압력이 일정하게 유지될 때 액체가 boiling(비등)하기 시작하면 전체가 완전 증발할 때까지 등온유지
3. 포화액-증기 혼합물 (Saturated liquid-vapor mixture) (=wet vapor, wet saturated vapor) :
상 변화가 일어나는 상태인, 액체와 증기상이 공존하는 화합물
1) Tsat =100℃ @1atm ⇒ 상변화(증발)가 진행 중에 있다.
2) quality : 0 < x < 1
4. (건)포화증기 [(dry) Saturated vapor ] :
온도를 조금만 낮춰도 쉽게 응축되는 증기
1) Tsat =100℃ @1atm
2) quality : x = 1(건도 100%)
5. 과열증기 (Superheated vapor) :
온도를 많이 낮춰도 쉽게 응축하지 않는 공기 (포화증기가 아닌 증기)
1) Tvapor(300℃) > Tsat @1atm
2) quality : 건도는 의미 없다.
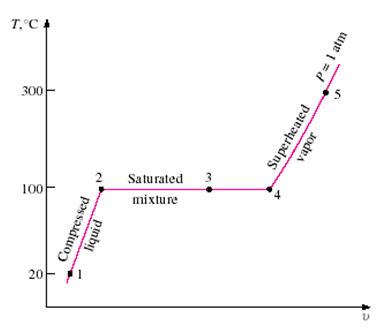
<그림 3> 일정 압력에서 물을 가열하는 과정에 관한 T-v 선도
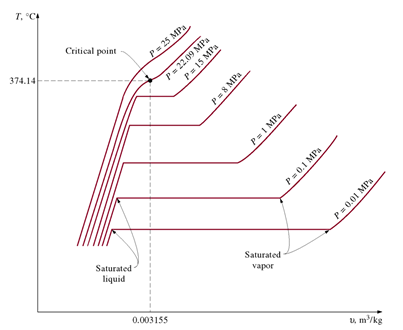
<그림 4> 압력변화에 따른 T-v 선도 (물의 예)
◇ 포화온도, 포화압력
▶ 포화 온도 Saturation temperature (Tsat) : 주어진 압력에서 순수물질이 상변화하는 온도
▶ 포화 압력 Saturation pressure (Psat) : 주어진 온도에서 순수물질이 상변화하는 압력
- 101.325 kPa의 압력에서 물의 Tsat는 99.97 ℃(약 100℃)이고,
99.97 ℃(약 100℃)에서 물의 Psat는 101.325 kPa임
- Tsat와 Psat의 관계
○ Tsat = f(Psat)
⇒ 상변화과정 동안에 압력과 온도는 종속상태량이다.
○ 높은 압력에 있는 물질은 높은 온도에서 끓게 된다. (예: 압력밥솥, 고산지대)
⇒ 이탈 분자가 압력을 이기려면 더 큰 에너지가 필요하므로
○ Psat를 일정하게 유지하려면 대기와 공기를 통하게 해 대기압으로 맞춰주면 됨
○ 포화압력이 높을수록 증발열이 감소함
◇ 잠열, 현열
▶ 잠열 latent heat : 상변화 과정 동안 흡수되거나 방출되는 에너지의 양
① 융해잠열 (용해잠열 혹은 용융잠열 latent heat of fusion) : 어는(녹는) 과정에서 흡수되는 에너지
② 증발잠열 (기화잠열 latent heat of vaporization) : 기화 동안에 흡수된 에너지의 양
( = 응축되는 동안 방출되는 에너지의 양)
* 물의 융해잠열 333.7 kJ/kg; 기화잠열 2257.1kJ/kg
* 잠열의 크기는 상변화에서 발생하는 온도 또는 압력에 의존한다.
▶ 현열(Sensible Heat)
= 질량*비열(Cp)*ΔT
- 현열은 열이 온도를 변화시키지만 잠열은 열이 상태를 변화 시킴
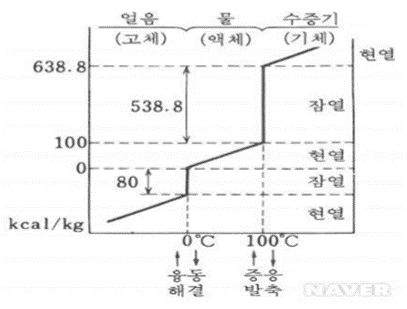
<그림 5> 물의 상태 변화도
'공학 기술 > 공학기본' 카테고리의 다른 글
| 상태량 표(열역학 성질표) (0) | 2021.12.03 |
|---|---|
| 상변화 과정에 대한 상태량 선도 (0) | 2021.12.01 |
| 순수물질의 상 (0) | 2021.11.30 |
| 열전달의 장애물 (0) | 2021.11.30 |
| 열매체의 종류 (0) | 2021.11.30 |





댓글