“가스 또는 증기의 상대밀도(Relative density of a gas or a vapor)”이라 함은 같은 압력과 온도에서 공기 밀도(공기 1.0)에 대한 가스 또는 증기의 상대 밀도를 말한다.

가스 또는 증기의 상대밀도
가스(Gas) vs. 증기(Vapor)
기체는 가스(Gas)와 증기(Vapor)로 나누어 생각 할 수 있다.
증기는 핵심은 액체이지만 기체 상태인 물질의 상태를 말하고, 반면에 기체는 전체적으로 가스 상태이다. 증기와 가스의 주요 차이점은 온도로서, 증기는 가스보다 온도가 낮다.
일반적으로 쉽게 다음과 같이 표현하기도 한다.
그 차이점은 가스는 상온 상압하에서 일정한 공간을 점유한 무정형 유체를 의미하면, 25℃, 1기압 상태에서 기체상태로 존재한다.
반면, 증기는 25℃ 기준 상온, 상압에서 액체 또는 고체로 존재하는 물질이 압력 강하(진공) 또는 온도상승(Thermal, E-Beam, Heat)으로 인해 기체 상태로 존재하는 유체로서 보통 기체와 액적이 섞여 있는 상태로 있게 된다.
- Vapor와 Gas의 주요 차이점은 Vapor는 물질의 상태이고 Gas는 요소(element)라는 것이다.
- 증기와 가스의 두 번째 차이점은 증기가 가스 분자보다 밀도가 낮다는 것이다.
- Vapor와 Gas의 세 번째 차이점은 둘 다 끓는점이 다르다는 것입니다. 액체에서 기체(증기)로 변하는 온도를 끓는점이라고 한다.
- 증기와 가스의 네 번째 차이점은 둘 다 비열 값이 다르다는 것입니다. 물질의 1g을 온도 1℃ 또는 K으로 변경하는 데 필요한 에너지의 양을 비열이라 한다.
- 증기와 가스의 다섯 번째 차이점은 증기가 더 쉽게 응축된다는 것이다. 증기를 응축할 수 있는 방법은 여러 가지가 있으며, 이를 통해 과학자들은 증기를 쉽게 액체나 고체로 되돌릴 수 있다.
가스 밀도(Gas Density)
가스 밀도에 대한 세부 내용은 기 포스팅한 다음 링크 자료 참조
https://sec-9070.tistory.com/1121
가스 밀도(Gas Density)
가스 밀도는 지정된 압력과 온도에서 특정 부피를 차지하는 가스의 질량으로 정의된다. 가스 밀도(Gas Density) 가스 밀도는 지정된 압력과 온도에서 특정 부피를 차지하는 가스의 질량으로 정의된
sec-9070.tistory.com
증기 밀도(Vapour Density)
증기 밀도 는 수소 와 관련된 증기의 밀도이다 . 특정 부피의 물질 질량을 같은 부피의 수소 질량으로 나눈 값으로 정의할 수 있다.
증기 밀도 = 기체 n 분자의 질량 / 수소 기체 n 분자의 질량 .
증기 밀도 = 기체의 몰 질량(molar mass) / H2 의 molar mass
증기 밀도 = 기체의 molar mass / 2.016
증기 밀도 = 1 ⁄ 2 × molar mass
(따라서: 몰 질량(molar mass) = ~2 × 증기 밀도)
* 예를 들어, NO2 와 N2O4 혼합물의 증기 밀도는 38.3이다. 증기 밀도는 차원이 없는 양(dimensionless)이다.
● 대체 정의(☞ 이는 아래의 상대밀도와 같은 개념)
그러나 많은 웹 소스에서, 특히 미국의 상업 및 산업 시설의 안전 고려 사항과 관련하여 증기 밀도는 수소가 아닌 공기와 관련하여 정의된다. 공기의 증기 밀도는 1로 지정된다. 이 용도에서 공기의 분자량은 28.97 a.m.u.(원자 질량 단위)이며, 다른 모든 기체 및 증기 분자량을 이 수로 나누어 증기 밀도를 구한다. 예를 들어 아세톤의 증기 밀도는 공기와 관련하여 2이다. 즉, 아세톤 증기는 공기보다 두 배 더 무겁다. 이는 아세톤의 분자량 58.1을 공기의 분자량 28.97로 나누면 2와 같다는 것을 알 수 있다.
이 정의에 따라 증기 밀도는 가스가 공기보다 밀도가 높은지(1보다 큰) 또는 밀도가 낮은지(1보다 작은)를 나타낸다. 밀도는 컨테이너 보관 및 작업자 안전에 영향을 미치는데, 용기가 밀도가 높은 가스가 누출된다면 그 증기는 가라앉고 가연성인 경우 발화하기에 충분한 농도가 될 때까지 모일 수 있다. 가연성이 아니더라도 밀폐된 공간의 낮은 층이나 바닥에 모여 공기를 대체하면 해당 공간의 낮은 부분에 들어가는 사람에게 질식 위험을 초래할 수 있다.
상대 밀도(Relative density)
상대 밀도는 주어진 기준(reference) 물질의 밀도에 대한 물질의 밀도 (단위 부피의 질량) 의 비율로 정의된다 .
따라서 증기 밀도와 마찬가지로 상대 밀도는 차원이 없는 양(dimensionless)이다.
액체의 경우에는 비중(specific gravity)이라고 하고, 비중은 거의 항상 밀도가 가장 높은 물 (4 °C 또는 39.2 °F) 을 기준으로 측정된다 .
가스의 경우 기준은 실온 (room temperature, 20 °C 또는 68 °F)의 공기로 한다.
물질의 상대 밀도가 1보다 작으면 기준 물질보다 밀도가 낮고, 1보다 크면 기준 물질보다 밀도가 높다. 상대 밀도가 정확히 1이면 밀도는 동일하다. 즉, 두 물질의 동일한 부피는 동일한 질량을 가진다. 기준 물질이 물이라면 상대 밀도(또는 비중)가 1보다 작은 물질은 물에 뜬다. 예를 들어 상대 밀도가 약 0.91인 각얼음은 뜬다. 상대 밀도가 1보다 큰 물질은 가라앉는다.
상대 밀도를 결정할 때에는 시료 및 기준 물질의 온도와 압력을 모두 지정하어야 한다.
그러나 일반적으로 압력은 거의 항상 1atm (101.325kPa) 이다 . 그렇지 않은 경우에는 밀도를 직접 지정하는 것이 더 일반적이다.
온도는 응용되는 산업계마다 다르므로 명시하여야 한다.
기체(가스 또는 증기)의 상대 밀도
IEC 61892-7에서는 기체의 상대밀도를 동일한 압력 및 동일한 온도에서 공기 밀도에 대한 가스 또는 증기의 밀도(공기는 1,0과 같음)로 정의하고 있다.
● Relative Density Information
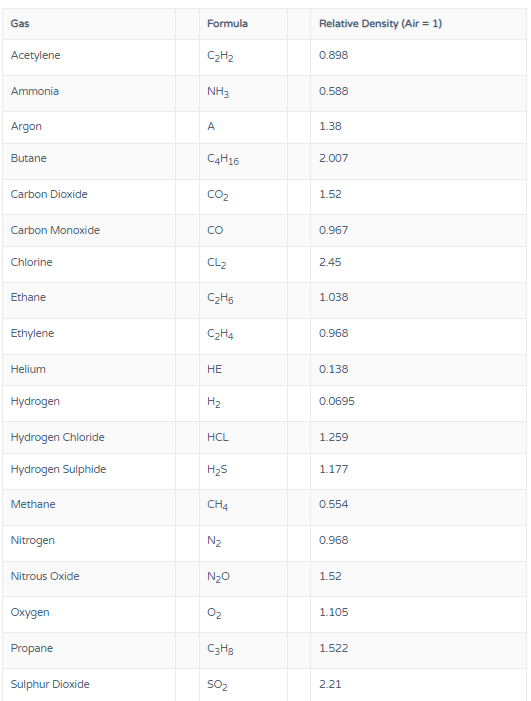
Source : https://www.ox-an.com/gas-density-data
Reference : 1. https://en.wikipedia.org/wiki/Vapour_density
2. https://en.wikipedia.org/wiki/Relative_density
3. https://www.ox-an.com/gas-density-data
'공학 기술 > 공학기본' 카테고리의 다른 글
| 증기 밀도 개념 및 활용 (0) | 2023.07.23 |
|---|---|
| 증기/공기 혼합물의 상대밀도 (0) | 2023.07.22 |
| 가스 밀도(Gas Density) (0) | 2023.07.20 |
| 공기의 밀도 (0) | 2023.07.19 |
| 분자량, 몰 질량 등 (0) | 2023.05.31 |





댓글