
사업장에서 사용하는 화학물질의 휘발성에 의해 그 유해위험도를 평가할 수 있다. 금번에는 사용하고 있는 물질이 저/중/고 휘발성 물질인지 판정하는 기준에 대해 공유하고자 한다.
휘발성(volatility) 정도 판정 기준
휘발성(volatility)
상온에서 액체나 고체가 기체가 되어 날아가 버리는 성질로, 끓는점이 낮은 액체 연료나 유기용제, 방향족 화합물 등이 강한 휘발성을 나타낸다.
일반적으로 액체의 표면에서 분자가 떨어져 나오는 현상, 즉 증발이 잘 일어나는 물질이 휘발성이 강하다. 따라서 휘발성이 강하다는 것은 증기압이 크다는 것을 의미하기도 한다. 액체의 경우 일반적으로 어느 정도 이상의 증기압을 지니지만, 액체 물질의 종류에 따라 증기압이 크게 달라지는데, 이는 극성이나 분자량에 따른 분자 간 인력이 다르기 때문이다. 고체 물질 역시 증기압을 나타내지만 액체에 비해 분자 결합이 단단하기 때문에 대개는 증기압의 크기가 매우 작다. 하지만 일부는 드라이아이스와 같은 큰 증기압을 갖는 고체가 존재하며, 이를 승화성 고체라 한다.
증기압, 온도 및 끓는점(Vapor pressure, temperature and boiling point)
물질의 증기압은 기체(증기)상이 액체 또는 고체상과 평형을 이루는 압력으로, 분자와 원자가 액체나 고체에서 빠져나가는 경향을 측정한 것이다 .
대기압에서 액체의 증기압이 온도가 증가함에 따라 대기압과 같아지는 지점까지 증가할 때, 액체는 끓는점, 즉 액체가 전체적으로 액체에서 기체로 상태가 변하는 온도에 도달하게 되는데, 이 온도를 일반적으로 액체의 정상 끓는점(normal boiling point) 이라고 한다 .
당연히 액체의 정상적인 끓는점은 온도가 낮을수록, 분자가 액체에서 빠져나가는 경향이 커지고 증기압도 높아진다. 즉, 액체의 증기압이 높을수록 휘발성이 높고 액체의 정상 끓는점이 낮다. 다음 그림은 다양한 액체에 대한 온도에 대한 증기압의 의존성을 나타내는 그래프로, 증기압이 높은 액체는 정상 끓는점이 낮음을 확인할 수 있다.

<그림 1> 다양한 액체의 증기압 그래프
예를 들어, 차트에 그래프로 표시된 액체 중 주어진 온도에서 가장 높은 증기압을 갖는 메틸 클로라이드(CH3Cl)는 증기압 곡선(파란색 선) 이 절대 증기압 의 1 기압 (atm) 의 수평 압력선과 교차하는 가장 낮은 정상 끓는점(-26°C)을 가지고 있다.
분자간 힘 의 관점에서, 끓는점은 액체 분자가 액체 내에서 분자를 서로 결합하는 다양한 분자간 인력을 극복하기에 충분한 운동 에너지 를 갖는 온도를 나타낸다. 따라서 끓는점은 이러한 인력의 강도를 나타내는 지표이기도 하다. 분자간 인력이 높을수록 분자가 액체에서 빠져 나오기가 더 어려워지고 따라서 액체의 증기압이 낮아진다. 액체의 증기압이 낮을수록 끓기 시작하려면 온도가 높아야 하고, 따라서 분자간 인력이 높을수록 정상 끓는점이 높아진다.
휘발성 및 증기압(Volatility and Vapor Pressure)
분자 수준에서 액체의 입자는 다양한 운동 에너지를 가지고 있다.
다음 그림과 같이 가장 활동적인 입자는 액체에서 빠져나와 기체 상태로 들어가기에 충분한 에너지를 가지고 있는데, 우리는 이것을 증발(evaporation)로 본다.

<그림 2> 증발 모형도
액체는 기체 상태로 들어가는 입자의 압력이 주변 대기압과 같아질 때 끓는다.
액체가 끓는점에 가까울수록 증기압이 높아지고, 끓는점이 낮은 액체는 끓는점이 높은 액체보다 주어진 온도에서 증기압이 더 높게 나타난다.
예를 들어 끓는점이 56°C인 아세톤은 물보다 증기압이 더 높다. 따라서 실온에서 아세톤은 물보다 더 많이 증기상으로 들어간다. 이것이 휘발성 액체의 특징이다.
MSDS의 증발 속도(evaporation rate)
일반적으로 증발율은 단위 시간당 표면적으로부터 증발되는 물질의 량(예 : grams per square meter per hour)을 의미하지만, 여기에서의 증발 속도는 알려진 특정 물질의 증발 속도와 비교하여 물질이 증발하는 상대적인 속도(액체에서 증기로 변화하는 증발) 비율을 의미하고 있어, 단위가 없다(unitless).
증발 속도는 물질의 건강 및 화재 위험을 평가하는 데 유용하게 사용할 수 있다. 예를 들어, 증발 속도가 높은 물질은 쉽게 흡입되거나 폭발 할 수 있는 증기를 형성한다 .
증발 속도는 일반적으로 끓는점과 반비례한다. 즉, 끓는점이 높을수록 증발 속도가 낮아진다.
증발 속도에 대한 일반적인 기준 물질은 아래와 같은 화학구조를 갖는 n - 부틸 아세테이트(일반적으로 BuAc로 약칭)가 사용되고 있다. 따라서 상대 증발 속도가 주어질 때마다 참조 물질이 명시되어야 한다.

<그림 3> n - 부틸 아세테이트 분자 구조식
따라서 BuAc의 상대 증발 속도는 1.0이 라고 할 때, 다른 재료는 다음과 같이 Fast, Medium, Slow로 분류된다.
<표 1> 증발속도 구분(Evaporation Rate Speed)

우리는 BuAc의 절대 증발 속도(즉, 질량/시간 단위)에 대한 특정 숫자를 알 수 없다. 아마도 그러한 수치는 온도, 대기압, 습도, 기류, 점도 등과 같은 무수한 변수에 따라 달라질 것이다.
그러나 참고로 ASTM은 표준 시험 방법인 D3539-87(2004) 휘발성 액체의 증발 속도에 대한 표준 시험 방법을 개발했으니 보다 자세히 알 필요가 있을 경우에는 이를 참조하기 바란다.
휘발성(volatility) 평가 기준
증발 속도 데이터가 없는 경우 재료의 증기압을 사용하여 휘발성을 대략적으로 평가할 수 있다.
다음 그림은 Clarke 사에서 사용하는 휘발성 액체의 Low, Medium, High Volatility 평가 기준이다.
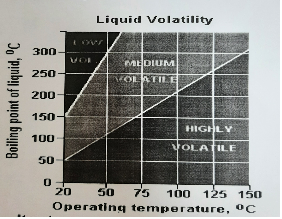
<그림 4> 액체의 휘발성 평가 기준(estimating volatility)
Reference : 1. https://en.citizendium.org/wiki/Volatility_(chemistry)
'공학 기술 > 공학기본' 카테고리의 다른 글
| 공기압 시스템 구성 (0) | 2022.07.17 |
|---|---|
| 국제단위(SI단위) (0) | 2022.07.17 |
| 감전의 기본 개념 (0) | 2022.07.12 |
| 용융도금업 특성 (0) | 2022.03.28 |
| 용융도금의 특성 (0) | 2022.03.28 |





댓글